
AND elementi
AND elementi məntiqi əlaqələrdə tətbiq edilən əsas rəqəmli məntiq elementidir –bu sağdakı riyazi cədvələ uyğun şəkildə özünü göstərir. Əgər AND elementində hər iki giriş maximum 1 olarsa , yalnız o zaman maxsimum çıxış 1 alınar. Əgər AND elementində yalnız bir giriş maxsimumdursa, nəticə minimum alınar.
== Simvollar ==
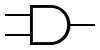
AND elementləri üçün 3 simvol var: Amerikan simvolu (ANSİ və ya "hərbi"), IEC (Avropa və ya düzbucaqlı), həmçinin də DIN simvolu.
AND elementi A və B girişləri və çıxış C ilə məntiqi ifadəni yerinə yetirir: C=A•B.
== Tətbiqləri ==
AND elementi adətən N-kanallı və ya P-kanallı metal oksid yarımkeçirici sahə effekti tranzistorularından (MOYSET) istifadə edilərək işlənib hazırlanır.Əsas rəqəmli girişlər a və b, çıxış F AND funksiyası kimi eyni nəticəyə malik olmalıdır.
== Alternativlər ==
Əgər heç bir səciyyəvi AND elementləri mövcud olmazsa, bir NAND və ya NOR elementlərindən hazırlana bilər, çünki NAND və NOR elementləri universal elementlər qəbul edilib.Buna görə də onlar başqalarının (başqa elementlərin) yerinə istifadə edilə bilər. Həmçinin XOR elementləri AND elementi ilə orşar istifadə edilə bilər,lakin nadir hallarda bunun üçün istifadə olunur.
Məntiq elementi
Məntiqi element — Bul funksiyasını yerinə yetirən fiziki qurğudur. O, bir və ya bir neçə məntiqi girişlərdə məntiqi əməliyyatı yerinə yetirir və sadə məntiqi çıxışları göstərir. Məntiq elementləri ilk növbədə elektron açarlar kimi fəaliyyət göstərən tranzistorlar və diodlar istifadə edərək yerinə yetirilir, həmçinin molekullar,optika, elektromaqnit relelər və hətta mexaniki elementlər istifadə edərək qurula bilər.
yapışdırıcı məntiq — (ing. glue logic, ru. связующая логика) – kompüterin bir əsas hissəsini başqa bir hissə ilə birləşdirmək üçün zəruri olan nisbətən sadə məntiqi sxemlər. Məsələn, mikroprosessorların bir çoxu mərkəzi prosessor (CPU) ilə yaddaş (MEMORY) arasında yapışdırıcı məntiqin olmasını tələb edir.
== Simvollar ==
== Ədəbiyyat ==
İsmayıl Calallı (Sadıqov), "İnformatika terminlərinin izahlı lüğəti", 2017, "Bakı" nəşriyyatı, 996 s.

NAND elementi
NAND elementi (İNKAR AND və ya NOT AND) — Rəqəmli elektronikada,yalnız bütün girişlər 1 (true) olanada, çıxışdakı məlumat 0 (false) alınan məntiqi element. Əgər hər iki giriş elementləri yalnız maxsimum 1 olarsa,nəticədə çıxış minimum-0 alınar. Əgər bir və ya hər iki giriş minimum 0 olarsa, nəticədə çıxış maxsimum-1 alınar. Bu tranzistorlarda istifadə edilir.
NAND elementləri əhəmiyyətlidir, çünki istənilən Bul funksiyası NAND elementlərinin kombinasiyasından istifadə edilərək yerinə yetirilə bilər.Bu xüsusiyyət funksional tamlıq adlanır. NOT(a1 AND a2 AND … AND an)funksiyası NAND(a1, a2, …, an) funksiyasının ekvivalentidir.
== Simvollar ==
NAND elementləri üçün 3 simvol var. MIL/ANSI simvolu, the IEC simvolu və DIN simvolu.
== Təhcizat təsviri və pinout ==
NAND elementləri əsas məntiqi elementlərdir və onlar TTL və CMOS İnteqral sxemlərdə tanınırlar.
== Tətbiqləri ==
NAND elementlərinin funksional tamlıqlarının xüsusiyyətləri var.Yəni ki,istənilən başqa məntiqi funksiyalar (AND,OR, və s.) yalnız NAND elementlərindən istifadə edərək yerinə yetirilə bilər.Tam prosessor tək NAND elementlərindən istifadə edilərək yaradıla bilər.

NOR elementi
NOR elementi — ortaq inkarı yerinə yetirən rəqəmli məntiq elementidir-bu sağdakı cədvələ uyğun şəkildə özünü göstərir. Əgər hər iki giriş elementləri minimum 0 olarsa, nəticədə çıxış maxsimum, yəni 1 alınar. Əgər bir və ya hər iki giriş maxsimum 1 olarsa, nəticədə çıxış minimum, yəni 0 alınar.
== Simvollar ==
NOR elementləri üçün üç simvol var:Amerikan simvolu (ANSİ və ya "hərbi"), IEC (Avropa və ya düzbucaqlı), həmçinin də DIN simvolu.

NOT elementi
Rəqəmli məntiqdə, çevirici və ya NOT elementi məntiqi inkarı yerinə yetirən məntiq elementidir (Cədvəl 1).
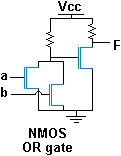
OR elementi
OR elementi məntiqi ayrılmanı yerinə yetirən rəqəmli məntiq elementidir.Əgər bir və ya hər iki giriş maxsimum 1 olarsa,nəticədə çıxış maxsimum 1 alınar.Əgər heç bir giriş maxsimum qiymət almazsa,nəticədə çıxış minimum-0 alınar.
== Simvollar ==
OR elementi üçün 3 simvol var: Alman(GNSI və "hərbi") simvolu, IEC simvolu və DIN simvolu.
== Tətbiqləri ==
== Alternativlər ==
Əgər heç bir müəyyən OR elementləri mümkün deyilsə,aşağıdakı şəkildə göstərilən konfiqurasiyada NAND və ya NOR elementlərindən istifadə edilə bilər.İstənilən məntiqi element NAND və ya NOR elementlərinin birləşməsindən hazırlana bilər.

XNOR elementi
XNOR elementi xüsusi OR elementinin tərsi olan funksiyanın rəqəmli məntiq elementidir.Sağdakı cədvələ uyğun şəkildə iki giriş versiyanın məntiqi ekvivalentliyini həyata keçirir.Əgər hər iki giriş elementi eyni olarsa, çıxış maxsimum-1 alınar.Əgər hər iki girişdən yalnız biri maxsimum(1) olarsa,nəticədə çıxış minimum (0) alınar.
== Simvollar ==
XNOR elementi üçün iki simvol var: xarakterik simvol və düzbucaqlı simvol.
== Alternativlər ==
Əgər heç bir müəyyən XNOR elementləri mümkün deyilsə,aşağıda göstərilmiş birləşmələrdə beş NAND elementindən və ya dörd NOR elementindən istifadə edilə bilər.Faktiki olaraq, istənilən məntiqi element yalnız NAND elementləri və ya yalnız NOR elementlərinin birləşməsindən hazırlana bilər.

XOR elementi
XOR elementi (bəzən EOR elementi və ya EXOR elementi adlanır) — xüsusi ayrılmanı (yəni, hər iki giriş fərqli olanda çıxışda 1 (true) alınan məntiqi əməliyyatdır) yerinə yetirən rəqəmli məntiq elementidir. Əgər girişlərdən yalnız hər hansı biri 1 olarsa, nəticədə çıxış maxsimum, yəni 1 (true) alınar. Əgər hər iki giriş minimum 0 (false) və ya hər ikisi 1 (true) olarsa, nəticə minimum 0 (false) alınar.
A
⋅
B
¯
+
A
¯
⋅
B
{\displaystyle A\cdot {\overline {B}}+{\overline {A}}\cdot B}
və
(
A
+
B
)
⋅
A
⋅
B
¯
{\displaystyle (A+B)\cdot {\overline {A\cdot B}}}
hər iki cəbri ifadə A və B girişləri olan XOR elementini təsvir edir.
== Simvollar ==
XOR elementi üçün iki simvol var: Ənənəvi simvol və IEEE simvolu.

Günəş
Günəş (simvoluəöö2ııeııe: ) – Günəş sisteminin mərkəzində yerləşən ulduzdur. Günəş orta ölçülü ulduz olmaqla Günəş sisteminin kütləsinin 99,8%-ni təşkil edir. Günəş radiasiyası formasında Günəşdən yayılan enerji Yerdəki həyatın var olmasına və iqlimə əsaslı təsir göstərir.
Bizim Qalaktikanın məlum olan təqribən 200 milyard ulduzundan biri olan Günəşin kütləsinin mütləq əksəriyyəti isti qazlardan ibarətdir. Günəş ətrafına istilik və işıq şəklində radiasiya yayır. Yerlə müqayisədə Günəşin diametri 109 dəfə, həcmi 1,3 milyon dəfə, kütləsi isə 333000 dəfə daha çoxdur. Günəşin sıxlığı Yerin sıxlığının 1/4-ü qədərdir. Günəş öz oxu ətrafında saatda 70000 km sürətlə hərəkət edir və bir dövrəsini təqribən 25 gündə tamamlayır. Günəşin səthinin istiliyi 5500 °C, nüvəsinin istiliyi isə 15,6 milyon °C-dir. Günəşdən ayrılan enerjinin 2,2 milyardda biri Yerə çatır.

Üzvi kimya
Üzvi kimya — tərkibində karbon atomu olan kimyəvi birləşmələri öyrənən bir elmdir. Üzvi kimya canlı aləmdə (bitki, heyvan, insan) yayılmış karbon atomunun digər 2 elementlərlə əmələ gətirdiyi birləşmələri öyrənən bir elimdir. Üzvi birləşmələri əmələ gətirən əsas dörd elementdir (O, H, N, C).
Üzvi kimya karbohidrogenləri və onların törəmələrini, yəni karbon əsaslı birləşmələri öyrənən kimya sahəsidir. Üzvi kimya maddələrin quruluşunu, xüsusiyyətlərini, reaksiyalarını və sintez yollarını araşdırır. Aşağıda üzvi kimyanın əsas aspektləri və sahələri haqqında məlumat verilmişdir:
Üzvi kimyanın əsas xüsusiyyətləri
1. Karbonun unikal rolu: Üzvi kimyada əsas element karbon atomudur. Karbon atomları öz aralarında və digər elementlərlə (hidrogen, oksigen, azot, kükürd, halogenlər və s.) sabit kovalent əlaqələr yarada bilir. Bu xüsusiyyət karbon birləşmələrinin müxtəlifliyini və mürəkkəbliyini təmin edir.
2.

Üzvi maddələr
Üzvi maddələr — biokütləni təşkil edən üzvü maddələrin cəmi, yəni orqanizmlərin canlı maddəsinin cəmi, orqanizmlərin ölü maddələri (töküntü, torf və s.), humus və ya çürüntü və ölü kütlənin parçalanması nəticəsində əmələ gələn çoxlu miqdarda məhsul (protein, karbohidratlar,
liqlin, yağlar, qətran, mum, üzvi turşular, aşılayıcı maddələr).
== Ümumi məlumat ==
Karbon atomunun üzvi birləşmələrinin çox olması bir çox səbəblərdən asılıdır. Hazırda 13 mln-dan çox üzvi maddə mövcuddur.
Üzvi kimya bir çox elmlərlə əlaqəlidir. İlk növbədə q/üzvi kimya, biokimya, fiziki kimya, biologiya, fizika, anatomiya, fiziologiya, biotexnologiya, ekologiya və s. elmlərlə sıx əlaqəli inkişaf edir.
Üzvi kimyanın inkişafında bir çox alimlərin rolu, xidmətləri olmuşdur. Y. Sil, Ş. Jerar, E. Franklit, Kekule, A. Kuper, M. Lomonosov, A. M. Butlerov, M. Markovnikov, A. Zinin, N. Zelinski, Kuçerov. Azərbaycan alimlərindən Y. Məmmədəliyev, Ə. Quliyev, A. Məhərrəmov, M. Qulubəyov, Ş. Ömərov və başqalarının xidmətləri olmuşdur.
Müasir üzvi kimyanın qarşısında geniş imkanlar durur.
Üzvi sintez
Üzvi sintez – üzvi maddələrin sintez üsuludur. Üzvi kimyanın mühüm bir sahəsidir.
== Tarixi ==
XIX əsrin əvvəllərinə qədər vitarizm nəzəriyyəsinin təsviri ilə belə hesab edilirdi ki, üzvi birləşmələr canlı orqanizmdə xüsusi həyati qüvvənin iştirakı ilə alına bilər. Həmin əsrin əvvəllərindən başlayaraq aparılan üzvi birləşmələrin ilk sintezləri bu nəzəriyyənin əsassızlığın göstərdi və o andan etibarən qeyri üzvi maddələr olan disian və amonyakın qarşılıqlı təsirindən üzvi maddə olan karbamidin (sidik cövhərinin) alınması ilə üzvi kimyada üzvi sintezin əsas qoyuldu:
Göründüyü kimi ilk üzvi sintezlər o qədər də mürəkkəb olmayan birləşmələrin alınması ilə başlamış, lakin tədricən üzvi sintezlər mürəkkəbləşmiş bir neçə mərhələli olmuş və bir neçə təbii birləşmələrin alınması mümkün olmuşdur. 1904-cü ildə bu üsulla adrinalin sintez olunmuşdur.
Hal-hazırda üzvi sintez sahəsi inkişaf etdirilərək təsdiq edilmişdir ki, çoxmərhələli reaksiyalar əsasında ən mürəkkəb quruluşlu, xüsusi əhəmiyyət kəsb edən birləşmələri əldə etmək olur.
== Üzvi sintezin üsulları ==
Üzvi sintezin üsulları iki cürdür.
Retrosintetik sintez üsulu
Templat sintez üsulu
== Retrosintetik analiz üsulu ==
Hazırda üzvi sintezin elə imkanları vardır ki, ən mürəkkəb quruluşlu birləşmələri sintez etmək mümkün olur, hətta bu bir neçə yolla baş verir. Çoxvariantlı sintez imkanı olduqda, sintezin səmərəliliyi əlavə olaraq başlanğıc birləşmələrin, reagentlərin asan əldə olunması reaksiya şəraitinin sadəliyi, məqsədli məhsulların çıxımının yüksək olması və sair digər amillərlə müəyyən olunur.
XX əsrin ilk illərindən başlayaraq məqsədli molekulların sintezinin planlaşdırılmasına sistematik yanaşma üsulundan – retrosintetik analiz adlanan bir üsul tətbiq edilmişdir..

Eyvan (memarlıq elementi)
Eyvan (Farsca: ایوان eyvān, ərəbcə: إيوان Iwan) üzəri daha çox tağlarla örtülmüş; Üç tərəfi bağlı, bir tərəfi tam açıq olan bir memarlıq elementidir. Eyvana İran memarlığında, Səlcuq və Osmanlı memarlığında tez-tez rast gəlinir.
Azotlu üzvi birləşmələr
Azotlu üzvi birləşmələr — azot tərkibli birləşmələrə deyilir. Azotlu üzvi birləşmələr mühüm birləşmələrdən biridir.
Elementli üzvi birləşmələr
Elementli üzvi birləşmələr (EÜB) - Bu birləşmədə Karbon başqa birləşmələrdən fərqli olaraq atomlarla rabitələri mövcuddur.
== İzahı ==
Əksər üzvi maddələr orqanogen-atomlardan (C, H, O, N, S) ibarətdir.Sonralar müəyyənləşdirildi ki, bunlardansavayı üzvi birləşmələrin tərkibində silisium, bor, metal atomları və praktik olaraq bütün elementlər ola bilər. Orqanogenlərdən fərqli olan bu birləşmələr element-üzvi birləşmələr (EÜB) adlandırılmışdır. Onlar praktik olaraq üzvi və qeyri-üzvi birləşmələrin xassələrini özündə cəmləşdirirlər.
== Tarixi ==
Hər şey arsendən başlandı. tanınmış alman alimi R.Bunzen 1841-ci ildə dimetilarseni (CH3)2AsH (kakodil) almışdır. bu ona baha başa gəldi. O, gözünü itirmiş, lakin tədqiqatı davam etdirmişdir. 50-ci illərdə Bunzenin tələbəsi E.Frankland sink-, qalay-, civə-üzvi birləşmələri almağa müvəffəq olmuşdur. Sonralar element üzvi birləşmələri XX əsrin görkəmli alimləri Fridel Krafts, Tsiqler, natta, Qrinyar, Andrianov, Nesmyanov və b.

Halogenli üzvi birləşmələr
Halogenli üzvi birləşmələr - tərkibində Karbon - Halogen rabitəsi saxlayan birləşmələrə deyilir.
== Halogenli törəmələrin nomenklaturası ==
Halogenli törəmələr R-Hal kimi (Alk-Hal-alkilhalogenidlər və Ar-Hal-arilhalogenidlər üçün) ümumi formulaya malikdirlər. Sistematik nomenklatura ilə ad verərkən müvafiq doymuş karbohidrogenin adının əvvəlinə halogen atomunun yerini göstərmək şətrilə "xlor", "brom", "yod" - sözləri yazılır. halogen karbohidrogen zəncirinin hansı ucuna yaxındırsa, nömrələmə də ordan başlanır. Əgər zəncirdə ikiqat və üçqat rabitələr varsa, onda nömrələmə ondan başlanır. Əgər halogen zəncirdə yeganə əvəzləyicidirsə, müvafiq radikalın adının sonunda "xlorid", "florid", "bromid" və "yodid" sözlərini əlavə edirlər. Əgər ilkin karbohidrogenin bütün hidrogen atomları halogenlə əvəz olunubsa onda halogenli törəmənin adının əvvəlinə "per-" sözü əlavə edilir.
Bir sıra halogenli törəmələr üçün trival nomenklaturadan istifadə edilir.
== Halogenidlərin fiziki xassələri ==
Struktur quruluşuna görə alkil və arilhalogenidlərin qaynama və ərimə temperaturları müvafiq karbohidrogenlərdən böyükdür. Normal şəraitdə, ancaq ən kiçik halogenidlər: CH3F, C2H5F, C3H3F, CH3Cl, C2H5Cl, CH3Br qazdır.

Kükürdlü üzvi birləşmələr
Kükürdlü üzvi birləşmələr - tərkibində Karbon - Kükürd rabitəsi birləşdirən birləşmələrə deyilir.
== Təsnifat ==
== Əsas nümayəndələri ==
== Adlandırılması ==
Kükürd üzvi birləşmələri adlandırmaq üçün "tio" hissəciyindən istifadə edilir.Bu ikivalentli kükürd atomunu göstərir. Bundan başqa "tio" oksigenin kükürdlə əvəz olunmasını göstərir. Məsələn "ol" hidroksil qrupunu OH, "tiol" ilə -SH qrupunu, "on" karbonil qrupunu, "tion" ilə C=S qrupunu adlandırırlar.
"Tia" hissəciyi ("tio"dan fərqli olaraq) karbon atomunun kükürdlə əvəz olunmasını göstərir.
== Mənbə ==
S.F.Qarayev, U.B.İmaşev, G.M.Talıbov "Üzvi kimya", Bakı-2003.

Metal üzvi birləşmələr
Metal üzvi birləşmələr
Metal-üzvi kimya metal-üzvi birləşmələri öyrənir. Metal-üzvi birləşmələr (MÜB) üzvi qrupların bilavasitə metal atomu ilə metal-karbon rabitəsi vasitəsilə əmələ gətirdiyi birləşmələrdir. Əgər üzvi liqand keçid metal atomu ilə bilavasitə keçid metal–karbon rabitəsi ilə birləşibsə, belə birləşmələr keçid metalların metal-üzvi birləşmələri, əgər qeyri-keçid metalla birləşibsə, onda qeyri-keçid metalların metal-üzvi birləşmələri adlanır. Metalüzvi birləşmələrin kompleks birləşmələrdən fərqi odur ki, kompleks birləşmələrdə bilavasitə metal–karbon rabitəsi yoxdur. Bu baxımdan metal-üzvi birləşmələr kompleks birləşmələrin xüsusi formasıdır. Keçid metalların metal-üzvi birləşmələrinə maraq əsasən iki aspektlə (praktik və fundamental) əlaqədardır. Ən əvvəl bu komplekslərin tədqiqi keçid metal atomunun rabitə yaratma qabiliyyətini araşdırmağa və keçid metal-üzvi liqand arasındakı çox mərkəzli ikielektronlu rabitələrin xüsusiyyətlərini dərindən dərk etməyə imkan verir. İkincisi keçid metalların metal-üzvi birləşmələrinin perspektivli katalitik sistemlər olması ilə əlaqədardır. Məlumdur ki, keçid metallar əsasında alınmış homogen katalizatorlar çoxtonnajlı kimyəvi məhsulların — spirtlər, plastifikatorlar, sirkə turşusu, dərman maddələrinin və s. sintezində istifadə edilir.

Oksigenli üzvi birləşmələr
Oksigenli üzvi birləşmələr — molekulunda Karbon — Hidrogen, Karbon — Oksigen rabitəsi saxlayan birləşməyə deyilir.

Qeyri-üzvi birləşmə
Qeyri-üzvi birləşmə — üzvi olmayan mənasına gəlir. Biologiyada su, mineral, turşu, əsaslar, duzlar kimi orqanizmlərin quruluşunda olan ancaq canlı olmayan və ya bir canlı tərəfindən istehsal edilməmiş kimyəvi birləşmələrdir. Təbiətdən hazır olaraq alınır, qeyri-üzvi birləşmələrin istehsalı mümkündür.
Qeyri-üzvi birləşmələr, sıxlıqla karbon daşımayan molekullardır. Bunlara misal kimi, anionlar və kationlar olaraq təsnif edilən müxtəlif ion birləşmələr ilə kovalent birləşmələrin verə bilərik.
Fotosintez edə bilən canlılar (dəniz yosunları, bitkilər və sianobakteriya) qeyri-üzvi birləşmələri sintezləşdirərək üzvi maddələr yaradırlar.
Qeyri-üzvi birləşmələr canlı quruluşuna qatılır və metabolik reaksiyalarda tənzimləyici vəzifəsi görür.
Silisiumlu üzvi birləşmələr
Silisiumlu üzvi birləşmələr - tərkibində Karbon - Silisium rabitəsi olan birləşmələrə deyilir. Bəzən onları Silikonlar adlandırırlar.
Zərif üzvi sintez
Zərif üzvi sintez – çoxmərhələli reaksiyalar sxemi üzrə az miqdarda reaktivlərlə mürəkkəb quruluşa malik birləşmələrin sintez üsuludur.
== Zərif üzvi sintezin əsas üzvi sintezlə müqayisəsi ==
Onların arasında bir sıra fərqlərin olduğunu aşkara çıxarır.. Əsas üzvi sintezin məhsullarından fərqli olaraq zərif üzvi sintezin məhsulları çox diqqətlə təmizlənməlidirlər. Zərif üzvi sintezin istehsallarının həcmi əsas üzvi sintezinki ilə müqayisədə çox da böyük olmur. Zərif üzvi sintezin məhsulları öz çeşidinə görə çoxsaylı və rəngarəngdir, məhsulların dəyəri isə nisbətən yükskdir. Adətən bu sənaye sahəsini “Kiçik tonnajlı kimya” adlandırırlar.
== Zərif üzvi sintez üsulunun tətbiqi ==
Zərif üzvi sintez üsulu ilə ilk dəfə sintetik üzvi birləşmələr toxuculuq sənayesində tətbiq olunmuşdur. XIX əsrin axırlarında ilk sintetik dərman preparatı (E.Fişer) və sintetik boyaq maddəsi (U.Perkin) alındı və kimya-əczaçılıq sənayesi yarandı. XX əsrin ortalarındatəbii maddələrin nümayəndələri (vitaminlər, antibiotiklər) sintez olundu və tətbiq sahəsi tapdı. Sonralar zülallar, nuklein turşuları, lipidlər, karbohidratların ayrı-ayrı nümayəndələri və fraqmentləri sintez olundu.

Qeyri-üzvi birləşmələr
Qeyri-üzvi birləşmə — üzvi olmayan mənasına gəlir. Biologiyada su, mineral, turşu, əsaslar, duzlar kimi orqanizmlərin quruluşunda olan ancaq canlı olmayan və ya bir canlı tərəfindən istehsal edilməmiş kimyəvi birləşmələrdir. Təbiətdən hazır olaraq alınır, qeyri-üzvi birləşmələrin istehsalı mümkündür.
Qeyri-üzvi birləşmələr, sıxlıqla karbon daşımayan molekullardır. Bunlara misal kimi, anionlar və kationlar olaraq təsnif edilən müxtəlif ion birləşmələr ilə kovalent birləşmələrin verə bilərik.
Fotosintez edə bilən canlılar (dəniz yosunları, bitkilər və sianobakteriya) qeyri-üzvi birləşmələri sintezləşdirərək üzvi maddələr yaradırlar.
Qeyri-üzvi birləşmələr canlı quruluşuna qatılır və metabolik reaksiyalarda tənzimləyici vəzifəsi görür.
Qeyri-üzvi kimya
Qeyri-üzvi kimya — kimyanın bütün kimyəvi elementlərin və onların qeyri-üzvi birləşmələrinin quruluşunu, reaksiya qabiliyyəti və xassələrini öyrənən sahəsi. Bu sahə üzvi maddələr istisna olmaqla, bütün kimyəvi birləşmələri əhatə edir (adətən qeyri-üzvi kimi təsnif edilən bir neçə sadə birləşmə istisna olmaqla, karbonu ehtiva edən birləşmələr sinfi). Tərkibində karbon olan üzvi və qeyri-üzvi birləşmələr arasındakı fərqlər, bəzi fikirlərə görə, ixtiyaridir. Qeyri-üzvi kimya kimyəvi elementləri və onların əmələ gətirdiyi sadə və mürəkkəb maddələri (üzvi birləşmələr istisna olmaqla) öyrənir. Ən son texnologiya materiallarının yaradılmasını təmin edir. 2013-cü ildə məlum olan qeyri-üzvi maddələrin sayı 500 minə yaxındır.
Qeyri-üzvi kimyanın nəzəri əsasını dövri qanun və ona əsaslanan D.İ.Mendeleyevin dövri sistemi təşkil edir. Qeyri-üzvi kimyanın ən mühüm vəzifəsi müasir texnologiya üçün zəruri olan xassələrə malik yeni materialların yaradılması üsullarının işlənib hazırlanması və elmi əsaslandırılmasıdır.
== Tərifin tarixi ==
Tarixən qeyri-üzvi kimya adı canlı varlıqlar tərəfindən əmələ gəlməyən elementlərin, birləşmələrin və maddələrin reaksiyalarının öyrənilməsi ilə məşğul olan kimya hissəsinin ideyasından irəli gəlir. Bununla belə, 1828-ci ildə görkəmli alman kimyaçısı Fridrix Völer tərəfindən həyata keçirilən qeyri-üzvi birləşmə ammonium sianatdan (NH4OCN) karbamid sintezindən bəri cansız və canlı təbiətin maddələri arasındakı sərhədlər silindi.
